| BK-virus | |
|---|---|
 |
|
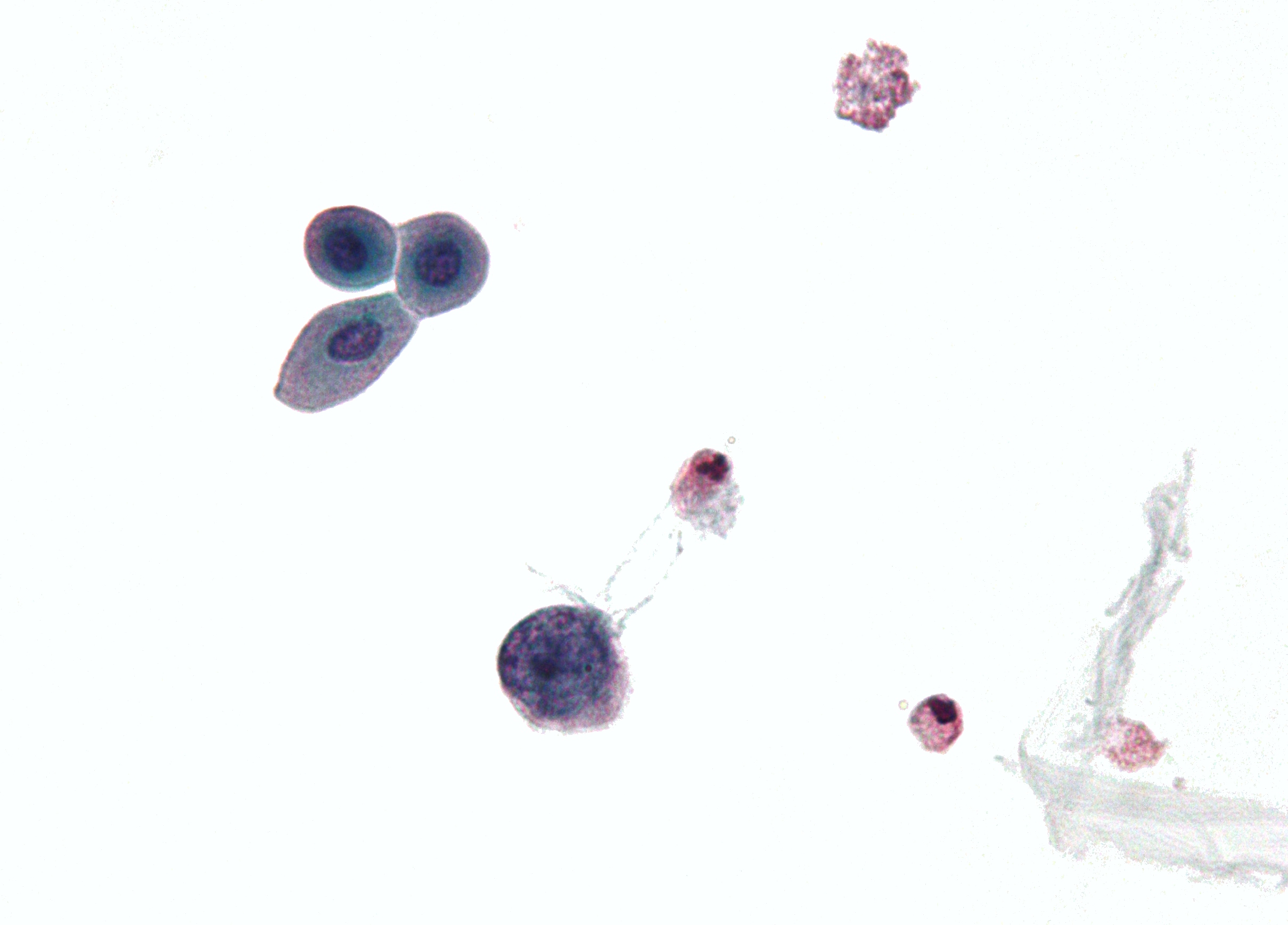
| Deze coupe toont een met polyomavirus geïnfecteerde cel – grote (blauwe) cel linksonder midden. Urinecytologie-exemplaar. | |
| Specialiteit | Besmettelijke ziekte |
De BK-virus is een lid van de polyomavirusfamilie. Infectie met het BK-virus is wijdverbreid, maar significante gevolgen van infectie zijn ongebruikelijk, met uitzondering van het immuungecompromitteerde en het immuunsysteem. BK-virus is een afkorting van de naam van de eerste patiënt van wie het virus in 1971 werd geïsoleerd (de patiënt was toen 29 jaar oud).
Symptomen van BK-virusinfectie
Het BK-virus veroorzaakt zelden ziekte, maar wordt meestal geassocieerd met patiënten die een niertransplantatie hebben ondergaan; veel mensen die met dit virus zijn geïnfecteerd, zijn asymptomatisch. Als er symptomen optreden, zijn deze meestal mild: luchtweginfectie of koorts. Dit zijn symptomen van primaire BK-infecties. Hoewel er geen klinische symptomen zijn, zijn voetafdrukken van het BK-virus aangetroffen in specimens van vrouwtjes die waren getroffen door een spontane abortus. Serumantistoffen tegen het BK-virus zijn ook gevonden bij spontane abortus getroffen vrouwen en bij vrouwen die een vrijwillige zwangerschapsonderbreking ondergingen.
Het virus verspreidt zich vervolgens naar de nieren en urinewegen waar het gedurende het leven van het individu blijft bestaan. Aangenomen wordt dat tot 80% van de bevolking een latente vorm van dit virus bevat, die latent blijft totdat het lichaam een of andere vorm van immunosuppressie ondergaat. Meestal is dit in de setting van niertransplantatie of multi-orgaantransplantatie. De presentatie bij deze immuungecompromitteerde personen is veel ernstiger. Klinische manifestaties zijn onder meer nierfunctiestoornissen (te zien aan een progressieve stijging van het serumcreatinine) en een abnormale urineanalyse die niertubulaire cellen en ontstekingscellen onthult.
Oorzaak
Virusoverdracht
Artsen weten niet hoe dit virus wordt overgedragen. Maar artsen weten dat het virus van persoon tot persoon wordt verspreid, en niet van een dierlijke bron. Er is gesuggereerd dat dit virus kan worden overgedragen via ademhalingsvloeistoffen of urine, aangezien geïnfecteerde individuen periodiek virus in de urine uitscheiden. Uit een onderzoek onder 400 gezonde bloeddonoren bleek dat 82% positief was voor IgG tegen het BK-virus.
Risicofactoren
Bij sommige niertransplantatiepatiënten heeft het noodzakelijke gebruik van immunosuppressiva als bijwerking dat het virus zich binnen het transplantaat kan vermenigvuldigen, een ziekte die BK-nefropathie wordt genoemd.
Van 1–10% van de niertransplantatiepatiënten evolueren naar BK-virus-geassocieerde nefropathie (BKVAN) en tot 80% van deze patiënten verliezen hun transplantaten. Het begin van nefritis kan al enkele dagen na de transplantatie optreden tot zelfs 5 jaar.
Het wordt ook geassocieerd met ureterstenose en interstitiële nefritis. Bij ontvangers van beenmergtransplantaties is het opmerkelijk als oorzaak van hemorragische cystitis.
BK-viremie-belasting> 185.000 kopieën / ml op het moment van de eerste positieve BKV-diagnose – de sterkste voorspeller voor BKVAN (97% specificiteit en 75% gevoeligheid). Bovendien bleken de BKV-virale ladingen in bloed die op elk moment 223.000 kopieën / ml bereikten, voorspellend te zijn voor BKVAN (91% specificiteit en 88% gevoeligheid).
Diagnose van BK-virusinfectie
Dit virus kan worden gediagnosticeerd door een BKV-bloedtest of een urinetest op lokcellen, naast het uitvoeren van een biopsie in de nieren. PCR-technieken worden vaak toegepast om het virus te identificeren.
Behandeling van BK-virusinfectie
De hoeksteen van therapie is het verminderen van immunosuppressie. Een recente stijging van BKVAN correleert met het gebruik van krachtige immunosuppressiva, zoals tacrolimus en mycofenolaatmofetil (MMF). Studies hebben geen correlatie aangetoond tussen BKVAN en een enkel immunosuppressivum, maar eerder de algehele immunosuppressieve belasting.
- Er zijn geen richtlijnen of medicijnniveaus en doses voor een juiste vermindering van immunosuppressiva bij BKVAN
- Meest voorkomende methoden:
- Intrekking van MMF of tacrolimus
- Vervanging van tacrolimus door cyclosporine
- Algehele vermindering van immunosuppressieve belasting
- Sommige ciclosporine-dalspiegels waren verlaagd tot 100-150 ng / ml en tacrolimus-spiegels verlaagd tot 3-5 ng / ml
- Retrospectieve analyse van 67 patiënten concludeerde dat transplantaatoverleving vergelijkbaar was tussen reductie en stopzetting van middelen.
- Onderzoek in één centrum toonde aan dat niertransplantaten werden behouden bij 8/8 personen die werden behandeld met een vermindering van de immunosuppressie, terwijl transplantaatverlies optrad bij 8/12 patiënten die werden behandeld met een toename van de therapie voor wat werd beschouwd als orgaanafstoting.
Andere therapeutische opties zijn onder meer Leflunomide, Cidofovir, IVIG en de fluorochinolonen. Leflunomide, een pyrimidinesyntheseremmer, wordt nu algemeen aanvaard als de tweede behandelingsoptie na vermindering van immunosuppressie.
Leflunomide in BKVAN
De grondgedachte achter het gebruik van leflunomide in BKVAN komt voort uit de gecombineerde immunosuppressieve en antivirale eigenschappen. Bij twee onderzoeken bestaande uit 26 en 17 patiënten die BKVAN ontwikkelden met een behandeling met drie geneesmiddelen van tacrolimus, MMF en steroïden, werd hun MMF vervangen door leflunomide 20-60 mg per dag. 84% en 88% van de patiënten hadden respectievelijk klaring of een progressieve vermindering van de virale belasting en een stabilisatie of verbetering van de transplantaatfunctie. In een studie uitgevoerd door Teschner et al. in 2009 hadden 12/13 patiënten die hun MMF hadden uitgewisseld met leflunomide het virus met 109 dagen geklaard. In een casusreeks was er verbetering of stabilisatie bij 23/26 patiënten met BKVAN na overschakeling van MMF op leflunomide.
Er zijn geen doseringsrichtlijnen voor leflunomide in BKVAN. De variabiliteit van patiënt tot patiënt heeft de dosering en monitoring van leflunomide buitengewoon moeilijk gemaakt.
- Onderzoek bij 26 en 17 patiënten kregen doses tussen 20 mg / dag en 60 mg / dag met dalspiegels van 50-100 µg / ml. Falen werd gezien bij patiënten met leflunomideplasmaspiegels <40 µg / ml.
- Een studie met 21 patiënten vond dat lage niveaus (<40 µg / ml) en hoge niveaus (> 40 µg / ml) vergelijkbare effecten hadden op de snelheid van virale klaring. Degenen met hogere niveaus hadden meer bijwerkingen (hematologisch, hepatisch).
- In de studie van Teschner et al. Vertoonden doseringen en geneesmiddelconcentratie geen correlatie met substantiële variatie van persoon tot persoon.
- In de Teschner-studie werden lage geneesmiddelconcentraties geassocieerd met een afname van de virale last. Dit maakt het moeilijk om te bepalen of verlaging van de viral load of toevoeging van leflunomide de oorzaak was van virale klaring.
Andere behandelingsopties
- Chinolonantibiotica: Ciprofloxacine (Cipro) bleek de virale last significant te verlagen, maar er zijn geen gegevens over overleving en transplantaatverlies.
- Intraveneuze immunoglobuline (IVIG) wordt gebruikt bij de behandeling van infectie en afstoting van allogene transplantaten – moeilijk te onderscheiden
- Cidofovir heeft beperkte gegevens en is zeer nefrotoxisch.
Geschiedenis
Het BK-virus werd voor het eerst geïsoleerd in 1971 uit de urine van een niertransplantatiepatiënt, initialen BK. Het BK-virus is vergelijkbaar met een ander virus dat het JC-virus (JCV) wordt genoemd, aangezien hun genomen een sequentieovereenkomst van 75% delen. Beide virussen kunnen worden geïdentificeerd en van elkaar worden onderscheiden door serologische tests uit te voeren met specifieke antilichamen of door een op PCR gebaseerde genotyperingsbenadering te gebruiken.
.













Discussion about this post